Setelah mengikuti pembelajaran siswa dapat :
1. menjelaskan pengertian entalpi suatu atom dan perubahannya,
2. menjelaskan pengertian reaksi eksoterm dan endoterm,
3. menentukan ΔH reaksi berdasarkan eksperimen kalorimeter dan hukum Hess,
4. menentukan ΔH reaksi berdasarkan data perubahan entalpi pembentukan standar dan data
energi ikatan
A. Sistem dan Lingkungan
Terjadinya perpindahan energi pada
sistem dan lingkungan dapat digambarkan seperti Gambar
perpindahan energi dari lingkungan ke sistem seperti gambar
1. Perubahan Entalpi
Perubahan energi pada suatu reaksi yang berlangsung pada tekanan tetap
disebut perubahan entalpi. Perubahan entalpi dinyatakan dengan lambang ΔH,
dengan satuan Joule dan kilo Joule.
Contoh:
Entalpi air ditulis HH2O. Air dapat berwujud cair dan padat. Entalpi yang dimilikinya
berbeda, HH2O(l) lebih besar daripada HH2O(s) . Oleh karena itu untuk mengubah
es menjadi air diperlukan energi dari lingkungan.
Harga ΔH pada peristiwa perubahan es menjadi air adalah:
ΔH = HH2O(l) – HH2O(s)
Perubahan ini dapat ditulis dalam suatu persamaan reaksi yang disebut
persamaan termokimia sebagai berikut.
H2O(s) → H2O(l) ΔH = +6,02 kJ
Berdasarkan perubahan entalpi, dikenal dua macam reaksi yaitu reaksi
eksoterm dan reaksi endoterm
1. Reaksi Eksoterm
Panas dihasilkan dari zat-zat bereaksi yang merupakan sistem kemudian
dilepaskan ke lingkungan. Reaksi ini termasuk reaksi eksoterm. Pada reaksi
eksoterm energi panas atau kalor berpindah dari sistem ke lingkungan.
Entalpi sistem sebelum reaksi lebih besar daripada sesudah reaksi atau
H pereaksi > H hasil reaksi
lebih kecil dari 0 atau ΔH = –.
Penulisan persamaan termokimianya
yaitu:
CaCO3(s) + H2O(l) → Ca(OH)2(aq) +
CO2(g)
ΔH = –97,37 kJ
Proses eksoterm dapat digambarkan
2. Reaksi Endoterm
Reaksi endoterm kebalikan dari
reaksi eksoterm. Padareaksi endoterm
sistem menyerap panas dari lingkungan.
Entalpi sistem sesudah reaksi
lebih besar daripada sebelum reaksi:
Hpereaksi < Hhasil reaksi.
Perubahan entalpi sistem menjadi lebih
besar dari 0 atau ΔH = +.
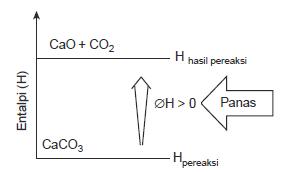
Perhatikan proses endoterm pada
reaksi CaCO3 menjadi CaO + CO2 seperti pada gambar
Untuk mengubah CaCO3(s) menjadi batu gamping (CaO) dan gas CO2
diperlukan energi panas. Persamaan termokimianya:
CaCO3(s) →CaO(s) + CO2(g) ΔH = +178,3 kJ
3. Macam-Macam Perubahan Entalpi (ΔH)
a. Perubahan Entalpi Pembentukan Standar (ΔHf)
Perubahan entalpi pembentukan standar, ΔHf suatu zat adalah perubahan
entalpi yang terjadi pada pembentukan 1 mol zat dari unsur-unsurnya diukur padakeadaan standar
Contoh:
1) Perubahan entalpi pembentukan AgCl adalah perubahan entalpi dari reaksi:
Ag(s) + 1/2 Cl2(g) ΔAgCl(s) ΔH = -127 kJ mol-1
2) Perubahan entalpi pembentukan KMnO4 adalah perubahan entalpi dari reaksi:
K(s) + Mn(s) + 2 O2(g) →KMnO4(s) ΔH = -813 kJ mol-
b. Perubahan Entalpi Penguraian Standar ΔHd
Perubahan entalpi penguraian standar merupakan kebalikan dari perubahan
entalpi pembentukan.
ΔHd suatu zat adalah perubahan entalpi yang terjadi pada reaksi penguraian
1 mol zat menjadi unsur-unsur pada keadaan standar
Contoh:
H2O(l) → H2(g) + 1
2 O2(g) ΔHd= +285,8 kJ mol–1
CO2(g) → C(s) + O2(g) ΔHd = +393,5 kJ mol–1
Marquis de Laplace dari Prancis dalam penelitiannya menemukan bahwa
jumlah kalor yang dibebaskan pada pembentukan senyawa dari unsur-unsurnya
sama dengan jumlah kalor yang diperlukan pada penguraian senyawa tersebut
menjadi unsur-unsurnya. Pernyataan ini dikenal sebagai Hukum Laplace.
Contoh:
1/2 N2(g) + 3/2H2(g) → NH3(g) ΔHf = -46,11 kJ
NH3(g) → 1/2 N2(g) + 3/2H2(g) ΔHd = +46,11 kJ
c. Perubahan Entalpi Pembakaran ΔHc
Perubahan entalpi pembakaran, ΔHc adalah perubahan entalpi yang terjadi
pada pembakaran 1 mol unsur atau senyawa pada keadaan standar.
Contoh:
CH4(g) + 2 O2(g) → CO2(g) + 2 H2O(l) ΔHc = -889,5 kJ
C2H2(g) + 5/2O2(g) →2 CO2(g) + H2O(g) ΔHc= -129,9
d. Perubahan Entalpi Netralisasi ΔHn
Perubahan entalpi netralisasi adalah perubahan entalpi yang terjadi pada
saat reaksi antara asam dengan basa baik tiap mol asam atau tiap mol basa.
Contoh:
NaOH(aq) + HCl(aq) →NaCl(aq) + H2O(l) ΔHn = -57,1 kJ mol-1
C. Penentuan ΔH Reaksi
Perubahan entalpi (ΔH) suatu reaksi dapat ditentukan melalui berbagai cara
yaitu melalui eksperimen, berdasarkan data perubahan entalpi pembentukan (ΔHf)berdasarkan hukum Hess, dan berdasarkan energi ikatan.
1. Penentuan ΔH Melalui Eksperimen
Perubahan entalpi reaksi dapat
ditentukan dengan menggunakan suatu
alat yang disebut kalorimeter (alat
pengukur kalor). Dalam kalorimeter, zatyang akan direaksikan dimasukkan ke
dalam tempat reaksi. Tempat ini dikelilingi
oleh air yang telah diketahui massanya.
Kalor reaksi yang dibebaskan terserap
oleh air dan suhu air akan naik. Perubahan
suhu air ini diukur dengan termometer.
Kalorimeter ditempatkan dalam
wadah terisolasi yang berisi air untuk menghindarkan terlepasnya kalor.
Jumlah kalor yang terserap ke dalam air dihitung dengan mengalikan 3 faktor
yaitu massa air dalam kalorimeter (gram), perubahan suhu air (Δt), dan kalor
jenis air. Rumusnya ditulis: q = m.c.Δt
q = kalor yang dibebaskan atau diserap
m = massa air (gram)
c = kapasitas kalor air (J)
Δt = perubahan suhu (°C)
Contoh Soal
Di dalam kalorimeter terdapat zat yang bereaksi secara endoterm. Reaksi tersebut
menyebabkan 1 kg air yang terdapat dalam kalorimeter mengalami penurunan
suhu 5C. Tentukan kalor reaksi dari reaksi tersebut!
Penyelesaian:
q = m.c.Δt
= 1.000 g. 4,2Jg-1° C-1. 5°C
= 21.000 J = 21 kj
Contoh Soal
50 mL larutan HCl 1M yang suhunya 22°C dicampurkan dengan 50 mL larutan
NaOH 1 M yang suhunya 22°C. Pada reaksi tersebut terjadi kenaikan suhu sampai
28,87°C. Tentukan, ΔHR netralisasi dan tulis persamaan termokimia reaksi tersebut.
Penyelesaian:
Jumlah mol HCl = 50 mL x 1 M = 50 mmol = 0,05 mol
Jumlah mol NaOH = 50 mL x 1 M = 50 mmol = 0,05 mol
Volum larutan = volum air = 100 mL
Massa larutan = massa air = 100 mL x 1 gmL–1 = 100 g
q = m x c x Δt
= 100 g x 4,2 J.g–1 °C–1.(28,87 °C – 22 °C)
= 2885,4 J = 2,8854 kJ
ΔHR = –q
ΔHR untuk 0,05 mol H2O = –2,8854 kJ
ΔH reaksi untuk 1 mol H2O =2,8854 kJ
0,05 mol = –57,71 kJ mol–1
Persamaan termokimianya:
HCl(aq) + NaOH(aq) → NaCl(aq) + H2O(l) ΔHR = –57,71 kJ mol–1.
2. Penentuan ΔH Berdasarkan ΔHf°
Berdasarkan perubahan entalpi pembentukan standar zat-zat yang ada dalam
reaksi, perubahan entalpi reaksi dapat dihitung dengan rumus:
ΔHR° = ΔHf°hasil reaksi – ΔHf°pereaksi
ΔHR° = perubahan entalpi reaksi standar
Contoh Soal
Tentukan ΔH reaksi pembakaran C2H6 jika diketahui:
ΔHf°C2H6 = –84,7 kJ mol–1, ΔHf°CO2 = –393,5 kJ mol–1, ΔHf°H2O = –285,8 kJ mol–1
Penyelesaian:
C2H6(g) + 3 1/2 O2(g) → 2 CO2(g) + 3 H2O(l)
ΔHRC2H6 = [2.ΔHf°CO2(g) + 3.ΔHf°H2O(l)] – [ΔHf°C2H6(g) + 3 1/2ΔHf°O2(g)]
= [2.(–393,5) + 3. (–285,8)] – [–84,7 + 0] = –1559,7 kJ
Jadi, ΔH pembakaran C2H6 adalah –1559,7 kJ
3. Penentuan ΔH Berdasarkan Hukum Hess
Perubahan entalpi reaksi kadang-kadang tidak dapat ditentukan secara
langsung tetapi harus melalui tahap-tahap reaksi. Misalnya untuk menentukan
perubahan entalpi pembentukan CO2 dapat dilakukan dengan berbagai cara.
Cara 1 C(g) + O2(g) →CO2(g) ΔH = -394 kJ
Cara 2 C dengan O2 bereaksi dulu membentuk CO, tahap berikutnya CO
bereaksi dengan O2 menghasilkan CO2.
Perhatikan diagram berikut
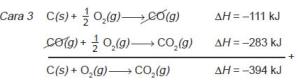
Pada cara 1, reaksi berlangsung satu tahap, sedangkan cara 2 dan cara 3
berlangsung dua tahap. Ternyata dengan beberapa cara, perubahan entalpinya
sama yaitu –394 kJ.
Seorang ilmuwan, German Hess, telah melakukan beberapa penelitian
perubahan entalpi ini dan hasilnya adalah bahwa perubahan entalpi reaksi dari
suatu reaksi tidak bergantung pada jalannya reaksi, apakah reaksi tersebut
berlangsung satu tahap atau beberapa tahap. Penemuan ini dikenal dengan Hukum
Hess yang berbunyi:
Perubahan entalpi hanya bergantung pada keadaan awal dan keadaan akhir
reaksi.
Contoh Soal
Tentukan perubahan entalpi pembentukan gas SO3 jika diketahui:
S(s) + O2(g) → SO2(g) ΔH = –296,8 kJ
SO2(g) + 1/2 O2(g) → SO3(g) ΔH = –99,2 kJ
Penyelesaian
4. Penentuan ΔH Berdasarkan Energi Ikatan
Suatu reaksi kimia terjadi akibat pemutusan ikatan-ikatan kimia dan
pembentukan ikatan-ikatan kimia yang baru. Pada waktu pembentukan ikatan
kimia dari atom-atom akan terjadi pembebasan energi, sedangkan untuk
memutuskan ikatan diperlukan energi. Jumlah energi yang diperlukan untuk
memutuskan ikatan antaratom dalam 1 mol molekul berwujud gas disebut energi
ikatan. Makin kuat ikatan makin besar energi yang diperlukan
Beberapa harga energi ikatanΔ
Harga energi ikatan dapat dipakai untuk menentukan ΔH suatu reaksi.
ΔHR = ∑ energi ikatan yang diputuskan – ∑ energi ikatan yang dibentuk
Contoh Soal
1. Dengan menggunakan harga energi ikatan, hitunglah ΔH reaksi:
CH4(g) + 4 Cl2(g) →CCl4(g) + 4 HCl(g
Energi ikatan yang diputuskan: Energi ikatan yang dibentuk:
4C – H = 4 . 415 = 1660 kJ 4C – Cl = 4 . 330 = 1320 kJ
4Cl – Cl = 4 . 243 = 972 kJ 4H – Cl = 4 . 432 = 1728 kJ
2632 kJ 3048 kJ
ΔH reaksi = 2632 kJ – 3048 kJ
= –416 kJ
D. Kalor Pembakaran
Kalor pembakaran adalah kalor yang dibebaskan apabila 1 mol bahan bakar
terbakar dengan sempurna dalam oksigen berlebihan
CH4(g) + 2 O2(g) → CO2(g) + 2 H2O(l) ΔH = -889 kJ
C3H8(g) + 5 O2(g)→ 3 CO2(g) + 4 H2O(l) ΔH = -1364 kJ
Selain energi panas, pembakaran ada juga yang menghasilkan energi bunyi
dan energi cahaya, seperti kembang api dan petasan.
Kalor pembakaran beberapa bahan bakar dapat dilihat pada Tabel
Cara sederhana untuk menghitung kalor pembakaran suatu bahan bakar dapat
dilakukan dengan percobaan sebagai berikut
Penentuan Kalor Pembakaran Etanol
Cara kerja
1. Masukkan 100 mL air ke dalam bejana dari tembaga, ukur suhu awal air.
2. Masukkan 100 mL etanol ke dalam pembakar, timbang etanol dengan
alat pembakar.